脊柱损伤护理的目标包括防止在评估和处置过程中进一步损伤;鉴别脊椎损伤,记录临床发现;优化神经功能恢复的条件;维护和恢复脊柱序列;尽可能避免脊柱活动能力损失;脊柱稳定和愈合;促进康复。[52]Bucholz RM, Heckman JD. Rockwood and Green's fractures in adults, 5th ed. Philadelphia, PA: Lippincott Williams & Wilkins; 2002:1303.
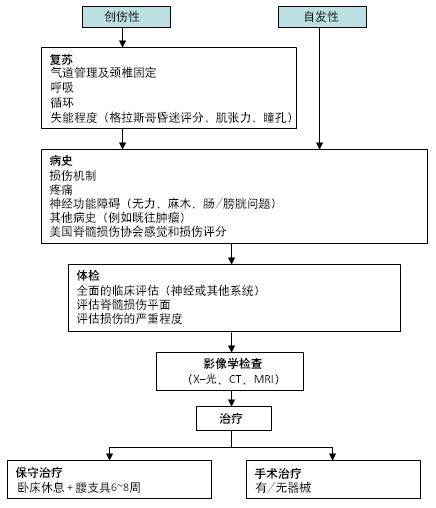 [Figure caption and citation for the preceding image starts]: 胸腰段椎体骨折的治疗B. Nurboja博士创建 [Citation ends].
[Figure caption and citation for the preceding image starts]: 胸腰段椎体骨折的治疗B. Nurboja博士创建 [Citation ends].
现场观察:可能是脊柱损伤
现场初步处理包括固定颈椎维持气道畅通后评估呼吸和通气,以及采取出血控制措施后评估血液循环情况。[28]American College of Surgeons. Advanced trauma life support manual, 7th ed. Chicago, IL: American College of Surgeons; 2004. 如持续出血,采用低血压复苏策略来将目标平均动脉血压维持在 50 到 65 mmHg。[30]Bickell WH, Wall MJ Jr, Pepe PE, et al. Immediate versus delayed fluid resuscitation for hypotensive patients with penetrating torso injuries. N Engl J Med. 1994 Oct 27;331(17):1105-9.http://www.nejm.org/doi/full/10.1056/NEJM199410273311701#t=articlehttp://www.ncbi.nlm.nih.gov/pubmed/7935634?tool=bestpractice.com[31]Morrison CA, Carrick MM, Norman MA, et al. Hypotensive resuscitation strategy reduces transfusion requirements and severe postoperative coagulopathy in trauma patients with hemorrhagic shock: preliminary results of a randomized controlled trial. J Trauma. 2011 Mar;70(3):652-63.http://www.ncbi.nlm.nih.gov/pubmed/21610356?tool=bestpractice.com 为改善灌注,在急性脊髓损伤后最初 7 天,平均动脉压应维持在 85 至 90 mmHg。[32]Blood pressure management after acute spinal cord injury. Neurosurgery. 2002 Mar;50(3 Suppl):S58-62.http://www.ncbi.nlm.nih.gov/pubmed/12431288?tool=bestpractice.com 在脊髓损伤后的急性期内,静脉使用吗啡为缓解疼痛的一线药物。 静脉使用氯胺酮为二线药物;如果获得静脉使用通路有延迟,则也可以使用鼻内给药氯胺酮或二乙酰吗啡(如有)。
应将患者放到含有颈椎固定器的矫正板上(应注意,长时间(>6小时)在矫正板上固定不动会引起患者褥疮的风险增大)。[53]Curry K, Casady L. The relationship between extended periods of immobility and decubitus ulcer formation in the acutely spinal cord-injured individual. J Neurosci Nurs. 1992;24:185-189.http://www.ncbi.nlm.nih.gov/pubmed/1517663?tool=bestpractice.com 在必须进行直线式脊柱固定的胸椎或腰骶椎损伤评估期间,重大发现包括:[29]National Institute for Health and Care Excellence. Spinal injury: assessment and initial management. February 2016. https://www.nice.org.uk [internet publication].https://www.nice.org.uk/guidance/ng41
年龄 ≥ 65 岁并有胸椎或腰骶椎疼痛
严重损伤的警示性特征(例如从>3 m [>10 英尺] 的地方跌落;[33]Velmahos GC, Spaniolas K, Alam HB, et al. Falls from height: spine, spine, spine! J Am Coll Surg. 2006 Nov;203(5):605-11.http://www.ncbi.nlm.nih.gov/pubmed/17084320?tool=bestpractice.com 摔下时脚或者臀部先着地;骑马事故;速度>100 km/h [>60 英里/小时] 时发生机动车事故 [motor vehicle accident, MVA];从机动车中弹出的事故;患者躯干前面有安全带印迹的机动车事故 [与腰椎 Chance 骨折相关];背部疼痛、下肢神经功能障碍 [虚弱或麻痹、麻木] 或括约肌功能障碍)
异常神经系统体征(运动受限/感觉缺乏);(触诊时)脊柱产生新的畸形或者骨中线压痛;咳嗽时中线或者脊柱疼痛
坐下、站立或踏步时疼痛或者异常神经系统体征(如出现疼痛停止动作)
脊柱的另一个区域疑似脊柱骨折
既往存在脊柱病理学改变。
抵达医疗机构后,即使怀疑患者脊椎受伤,也应该立即拆下矫正板。
美国外科医师协会对成年患者的滚动手法(在保证脊柱不弯曲的情况下滚动患者)给出了以下建议(高级创伤生命支持,创伤委员会,2012年):
患者可能患有两种低血压中的一种。 这两种低血压都需要立即鉴别和进行治疗。
低血压,伴有心动过速
低血压,伴有心跳过缓或心率正常
这是神经性休克。
应采用补液/输血的治疗方法,但要注意不能造成液体过剩和肺水肿;如果症状持续,应开始进行血管加压处理。[28]American College of Surgeons. Advanced trauma life support manual, 7th ed. Chicago, IL: American College of Surgeons; 2004.
血管加压药最好在配有创血流动力监测设施的重症监护环境下使用。
损伤类型
单纯性前柱损伤
需要止痛,卧床休息1到3周。 疼痛缓解后可以开始在使用或不使用外部制动装置(支具)。的情况下活动 需要拍摄一系列X线片,排除进行性畸形的可能性。
对于难治性疼痛的患者或者椎体前呈楔形而椎体后方皮质完整的患者(这可避免水泥漏入椎管),[54]Greenberg MS. Handbook of neurosurgery, 6th ed. New York, NY: Thieme New York; 2005:747. 椎体成形术或后凸成形术可能是一种选择。
如果患者有以下不稳定的情况,也可能需要手术:[55]Hitchon PW, Jurf AA, Kernstine K, et al. Management options in thoracolumbar fractures. Contemp Neurosurg. 2000;22:1-12.
一处压缩性骨折,椎体高度缺失超过50%,有成角(特别是楔形的前部成为一点);1个节段的脊柱后凸成角>40°(或25%);或剩余椎管宽度≤正常值的50%
三处或更多处相邻椎体压缩性骨折
神经系统功能障碍
后柱断裂,或中柱损伤超过最低限度
进行性脊柱后凸(如果椎体前部损失的高度超过75%,发生进行性脊柱后凸的风险会升高;腰椎压缩性骨折发生进行性脊柱后凸的风险高于胸椎压缩性骨折)。[54]Greenberg MS. Handbook of neurosurgery, 6th ed. New York, NY: Thieme New York; 2005:747.
后柱损伤
骨折脱位
爆裂性骨折
如果存在部分神经功能障碍;畸形角度≥20%;剩余椎管直径≤正常值的50%;及/或前椎体高度≤后椎体高度的50%,则需要进行手术治疗。[55]Hitchon PW, Jurf AA, Kernstine K, et al. Management options in thoracolumbar fractures. Contemp Neurosurg. 2000;22:1-12.
骨质疏松性骨折和非骨质疏松性骨折
非骨质疏松性骨折
骨质疏松性骨折
有神经功能障碍的患者通常需要经皮治疗(椎体成形术(VP)或后凸成形术(KP)),特别是在疼痛影响患者的活动时。 但是,如果骨折伴有<5%到10%的椎体高度缺失,通常不考虑采用经皮治疗。 治疗的主要目的是固定椎体、防止脊柱后凸和缩短疼痛时间(由于骨折得到了固定)。
椎体成形术用于治疗骨折时间在1个月以内、椎体压缩<30%的痛感强烈的骨质疏松性的压缩性骨折。 使用椎体成形术时要经椎弓根向压缩的椎体注射聚甲基甲烯酸丙酯(PMMA)。
后凸成形术用于治疗骨折时间在3个月以内、椎体压缩≥30%的痛感强烈的骨质疏松性的压缩性骨折。[56]Lovi A, Teli M, Ortalina A, et al. Vertebroplasty and kyphoplasty: complementary techniques for the treatment of painful osteoporotic vertebral compression fractures: a prospective non-randomised study on 154 patients. Eur Spine J. 2009 Jun;18 Suppl 1:95-101.http://www.ncbi.nlm.nih.gov/pubmed/19437044?tool=bestpractice.com 使用后凸成形术时,需要在骨折的椎体内放入一个球囊并充气,恢复脊椎的高度,之后以低压注射粘性骨水泥。
进行经皮治疗的证据存在一些有争议的情况。 椎体成形术的安全性和有效性研究试验(INVEST)表明,对于采用椎体成形术和痛点注射治疗骨质疏松性骨折的临床效果而言,一年后两者并没有什么区别。[57]Comstock BA, Sitlani CM, Jarvik JG, et al. Investigational Vertebroplasty Safety and Efficacy Trial (INVEST): patient-reported outcomes through 1 year. Radiology. 2013 Oct;269(1):224-31.http://www.ncbi.nlm.nih.gov/pubmed/23696683?tool=bestpractice.com 但是,Vertos II(急性骨质疏松性椎体压缩性骨折的椎体成形术与保守疗法对比)试验表明,对于患有急性骨质疏松椎体压缩性骨折且持续疼痛的患者,经皮椎体成形术既有效又安全。 进行椎体成形术后可立刻止痛,有效期至少为一年,远远超过保守疗法的效果。[58]Klazen CA, Lohle PN, de Vries J, et al. Vertebroplasty versus conservative treatment in acute osteoporotic vertebral compression fractures (Vertos II): an open-label randomised trial. Lancet. 2010 Sep 25;376(9746):1085-92.http://www.ncbi.nlm.nih.gov/pubmed/20701962?tool=bestpractice.com
球囊扩张后凸成形术为治疗椎体压缩性骨折的住院患者提供了一种成本效益较高的可以替代保守疗法的方法。[59]Ström O, Leonard C, Marsh D, et al. Cost-effectiveness of balloon kyphoplasty in patients with symptomatic vertebral compression fractures in a UK setting. Osteoporos Int. 2010 Sep;21(9):1599-608.http://www.ncbi.nlm.nih.gov/pubmed/19924497?tool=bestpractice.com
如果患者没有神经功能障碍,则应首先尝试保守疗法。
经皮治疗的禁忌症包括严重的合并症(即患者的麻醉可能存在风险)、骨折完全痊愈(通常>3个月)、凝血性疾病、活动性感染、脊柱不稳定、骨折造成>80%的椎体高度损失(技术上有难度)、急性爆裂性骨折以及由于肿瘤或骨折碎片复位造成的严重椎管受压。
保守(非手术)治疗
适应症包括:
没有神经功能障碍;已治愈;或神经功能障碍与明显的压迫、畸形或不稳定无关
对位合适(最初或经过体位复位后)
压缩性骨折造成的椎体高度损失<50%
成角<20°
患者的手术入路区域有烧伤或皮肤缺损,血液动力学不稳定,患有脓毒症和/或其他严重的共病[60]Bucholz RM, Heckman JD. Rockwood and Green's fractures in adults, 5th ed. Philadelphia, PA: Lippincott Williams & Wilkins; 2002:1424-1434.
安全带损伤,但没有神经功能障碍或没有立即发生神经功能障碍的风险。 这些患者应在伸展位使用外固定治疗。[54]Greenberg MS. Handbook of neurosurgery, 6th ed. New York, NY: Thieme New York; 2005:747.
治疗意见包括:
卧床休息,注意褥疮、血栓栓塞(使用抗血栓栓塞压力袜或肝素)、呼吸问题和便秘的风险。
膀胱出现问题时使用导尿管插入术(对于慢性膀胱问题,使用耻骨上导尿管插入)。
服用通便药物防止便秘。
使用适当的营养品促进骨折和伤口愈合。
佩戴支具:尽管并未有研究证明其有效,但胸腰段椎体骨折中经常使用支具。[61]Giele BM, Wiertsema SH, Beelen A, et al. No evidence for the effectiveness of bracing in patients with thoracolumbar fractures. Acta Orthop. 2009;80:226-232.http://informahealthcare.com/doi/full/10.3109/17453670902875245http://www.ncbi.nlm.nih.gov/pubmed/19404808?tool=bestpractice.com 对胸腰段椎体骨折(无神经功能障碍)情况下使用支具和不使用支具进行的随机对照试验表明,两组的效果相当(在损伤后3个月进行的Roland Morris问卷评分结果)。[62]Bailey CS, Urquhart JC, Dvorak MF, et al. Orthosis versus no orthosis for the treatment of thoracolumbar burst fractures without neurologic injury: a multicenter prospective randomized equivalence trial. Spine J. 2014;14:2557-2564.http://www.ncbi.nlm.nih.gov/pubmed/24184649?tool=bestpractice.com
使用支具(腰背支具或熟石膏)6到8周,减小生理性负重。 经过一段时间后这些外部固定装置会变松,需要由临床医生进行调整。[60]Bucholz RM, Heckman JD. Rockwood and Green's fractures in adults, 5th ed. Philadelphia, PA: Lippincott Williams & Wilkins; 2002:1424-1434.
早期康复和物理治疗,以预防呼吸道问题(肺不张)和血栓栓塞。 但应注意在固定3个月后才能进行躯干伸展,以留出足够的愈合时间。
骨质疏松性骨折患者需要卧床休息7天,并佩戴腰支具6到8周。 某些情况下患者出院回家后还要佩戴腰支具。
手术治疗
以下情况下建议采用手术治疗:[60]Bucholz RM, Heckman JD. Rockwood and Green's fractures in adults, 5th ed. Philadelphia, PA: Lippincott Williams & Wilkins; 2002:1424-1434.
软组织损伤,除非韧带足够完好,否则无法康复
有证据表明神经功能恶化
疼痛加剧
椎体序列不齐程度进行性加重。
进行手术的目的包括恢复椎体序列、矫正畸形、神经结构减压以及稳定脊柱。
如果有放射学证据表明存在压缩骨折,而且神经功能障碍正在恶化,则应进行手术减压。[60]Bucholz RM, Heckman JD. Rockwood and Green's fractures in adults, 5th ed. Philadelphia, PA: Lippincott Williams & Wilkins; 2002:1424-1434.
如果存在胸腰/腰椎脱位、创伤性脊椎前移、非手术治疗失败或不能耐受非手术治疗(例如患者不能合作,年龄太小,痴呆,不能卧床休息或佩戴腰支具)等情况,则应进行手术稳定(使用棒和钉)。[60]Bucholz RM, Heckman JD. Rockwood and Green's fractures in adults, 5th ed. Philadelphia, PA: Lippincott Williams & Wilkins; 2002:1424-1434.
后侧/后外侧入路
前侧/前外侧入路
如果后侧稳定减压失败,而患者的部分神经功能障碍仍然存在,则通常将该方法作为第二选择使用。[63]Dunn HK. Anterior stabilization of thoracolumbar injuries. Clin Orthop Relat Res. 1984;189:116-124.http://www.ncbi.nlm.nih.gov/pubmed/6478689?tool=bestpractice.com[64]Benzel EC, Larson SJ. Functional recovery after decompressive operation for thoracic and lumbar spine fractures. Neurosurgery. 1986;19:772-778.http://www.ncbi.nlm.nih.gov/pubmed/3785624?tool=bestpractice.com
前侧骨折碎片造成椎管受压>30%(在这种情况下,椎板切除对降低接触负荷没有效果)的患者采用。[65]Allen BL Jr, Tencer AF, Ferguson RL. The biomechanics of decompressive laminectomy. Spine (Phila Pa 1976). 1987;12:803-808.http://www.ncbi.nlm.nih.gov/pubmed/3686236?tool=bestpractice.com
使患者侧卧于折叠手术台上,以展开肋骨。 在损伤平面的肋间隙进行开胸术。 然后找到各段血管并进行结扎。 可以将肋骨切除用于移植。 使用咬骨钳清除椎体的骨折碎片,同时注意保护前皮质,这样可以减少对大血管的损伤。 清理完椎体碎片后,使用移植骨进行椎体间关节融合。
联合入路[60]Bucholz RM, Heckman JD. Rockwood and Green's fractures in adults, 5th ed. Philadelphia, PA: Lippincott Williams & Wilkins; 2002:1424-1434.
后路使用的器械系统是基于骨性固定(钩和螺钉)和纵向构架(棒及钢板)。[60]Bucholz RM, Heckman JD. Rockwood and Green's fractures in adults, 5th ed. Philadelphia, PA: Lippincott Williams & Wilkins; 2002:1424-1434. 三维计算机辅助导航放置椎弓根螺钉可以提高精度,减少手术时间,并可在各段胸椎,特别是上胸椎上安全有效地进行。[66]Wu H, Gao ZL, Wang JC, et al. Pedicle screw placement in the thoracic spine: a randomized comparison study of computer-assisted navigation and conventional techniques. Chin J Traumatol. 2010;13:201-205.http://www.ncbi.nlm.nih.gov/pubmed/20670575?tool=bestpractice.com 前路使用的器械系统主要是基于钢板、棒、组合器械和椎体间器械。 各种器械的使用可能带来的并发症包括脑脊液(CSF)渗漏、深部术后感染、暂时性机能麻痹以及永久性神经根损伤。
有证据表明,在使用器械固定不稳定的胸腰段椎体骨折时使用经椎弓根体内植骨(TBG)可以降低失败率。[67]Ma Y, Li X, Dong J. Is it useful to apply transpedicular intracorporeal bone grafting to unstable thoracolumbar fractures? A systematic review. Acta Neurochir (Wien). 2012 Dec;154(12):2205-13.http://www.ncbi.nlm.nih.gov/pubmed/23053291?tool=bestpractice.com 经椎弓根体内植骨(TBG)是在使用器械固定恢复解剖对位后,将松质骨植入骨折部位。 有趣的是,有meta分析表明将短节段器械和长节段器械用作没有神经功能障碍的胸腰段椎体骨折的手术治疗方法时,两者并没有区别。[68]Cheng LM, Wang JJ, Zeng ZL, et al. Pedicle screw fixation for traumatic fractures of the thoracic and lumbar spine. Cochrane Database Syst Rev. 2013 May 31;(5):CD009073.http://onlinelibrary.wiley.com/doi/10.1002/14651858.CD009073.pub2/fullhttp://www.ncbi.nlm.nih.gov/pubmed/23728686?tool=bestpractice.com
对经过手术治疗的胸腰段椎体骨折进行的融合和非融合的meta分析比较表明,如果通过后侧椎弓根螺钉固定对腰胸椎爆裂性骨折进行了治疗,则不需要融合。[69]Tian NF, Wu YS, Zhang XL, et al. Fusion versus nonfusion for surgically treated thoracolumbar burst fractures: a meta-analysis. PLoS One. 2013 May 21;8(5):e63995.http://www.ncbi.nlm.nih.gov/pmc/articles/PMC3660321/http://www.ncbi.nlm.nih.gov/pubmed/23704968?tool=bestpractice.com 两组在放射预后、功能预后、神经系统预后和内植物失败率等方面没有显著差异。 此外,非融合还可以大幅缩短手术时间和失血量。
关于胸腰段椎体骨折和脊髓损伤患者的减压时机以及减压时机是否对结果有影响仍存在争议。 目前最好的证据来自于“急性脊髓损伤手术时机的研究”(STASCIS)。[70]Fehlings MG, Vaccaro A, Wilson JR, et al. Early versus delayed decompression for traumatic cervical spinal cord injury: results of the Surgical Timing in Acute Spinal Cord Injury Study (STASCIS). PLoS One. 2012;7(2):e32037.http://www.plosone.org/article/info%3Adoi%2F10.1371%2Fjournal.pone.0032037http://www.ncbi.nlm.nih.gov/pubmed/22384132?tool=bestpractice.com 这是一项前瞻性的观察队列研究,对早期接受手术(即受伤后<24小时)和晚期接受手术(即受伤后24小时或更长)的患者的神经系统预后进行了比较。 研究表明,在受伤后24小时内可以安全地进行减压,而且在6个月的随访中神经系统预后有改善。 早期手术组中报告的并发症率为24.2%,晚期手术组为30.5%。
前侧入路和后侧入路
meta分析没有发现使用前侧和后侧入路治疗胸腰椎爆裂性骨折在神经系统恢复、重返工作、并发症和Cobb角等方面存在差异。[71]Xu GJ, Li ZJ, Ma JX, et al. Anterior versus posterior approach for treatment of thoracolumbar burst fractures: a meta-analysis. Eur Spine J. 2013 Oct;22(10):2176-83.http://www.ncbi.nlm.nih.gov/pubmed/24013718?tool=bestpractice.com 与后侧入路相比,前侧入路所需的手术时间更长,失血量更大,成本也更高。 尽管后侧入路似乎比前侧入路更有效,但我们需要更高质量的随机临床试验来证实这一点。[71]Xu GJ, Li ZJ, Ma JX, et al. Anterior versus posterior approach for treatment of thoracolumbar burst fractures: a meta-analysis. Eur Spine J. 2013 Oct;22(10):2176-83.http://www.ncbi.nlm.nih.gov/pubmed/24013718?tool=bestpractice.com
胸腰段椎体骨折脱位手术
胸腰段椎体骨折脱位是不稳定的,对稳定脊柱的椎体和韧带造成严重损伤。 这种损伤的最佳治疗方法仍存在争议,包括多种手术,从联合前后入路(P-A)融合到经椎间孔入路椎体间融合(TTIF)。 一项随机对照试验发现,两种治疗方法在融合率、减压程度、矫正度丢失、器械失败率、美国脊髓损伤协会评分、视觉模拟量表评分以及Oswestry伤残指数等方面都是相似的。 但是,P-A组的失血量、手术时间和围手术期并发症率都高于TTIF组。[72]Hao D, Wang W, Duan K, et al. Two-year follow-up evaluation of surgical treatment for thoracolumbar fracture-dislocation. Spine (Phila Pa 1976). 2014 Oct 1;39(21):E1284-90.http://www.ncbi.nlm.nih.gov/pubmed/25077910?tool=bestpractice.com
镇痛
最常用于肌肉骨骼疼痛的镇痛药物包括非甾体抗炎药(NSAID)、扑热息痛和阿片类镇痛药,取决于疼痛的严重程度。
深静脉血栓的预防
建议适当的 DVT 预防,以防止出现 DVT 和肺栓塞。 在受伤的72小时内,应开始使用压力袜和进行长期抗凝治疗,使用低分子量肝素或调整剂量的普通肝素。 弹力袜应当持续使用 2 周。 抗凝治疗应当持续使用 8 周。 但是,如果存在血栓栓塞的其他风险 (例如下肢骨折、血栓病史、癌症、心力衰竭、肥胖或年龄>70 岁),抗凝治疗应当继续使用 12 周或直至出院。
褥疮
在脊髓损伤后,由于以下因素,发生褥疮有极高的风险:
感觉缺失,使得患者不知道褥疮的发展
损伤平面以下缺乏肌肉运动
血液循环受损,从而降低了对皮肤的输氧量。
褥疮可能会使患者的治疗时间推迟数周,并留下永久性易受感染的瘢痕。 患者应定期安全地翻身,减少身体任何一侧承受的压力;应定期对皮肤进行检查,确认是否有褥疮的症状。 通常情况下,将患者翻身30º,并用枕头提供适当的支撑即可。 脚跟应离开床,用枕头支撑。 如果脊柱不稳定,则不能使用活动床垫等减压装置;而且这些装置对于脊髓损伤患者预防褥疮也没有什么效果。 儿童褥疮通常是由于支具和夹板等设备的压力以及丢在、忘在床上或椅垫上的玩具引起的。 患者绝对不能坐在或躺在褥疮伤口上。[73]London Spinal Cord Injury Centre, National Spinal Cord Injury Board. Spinal cord injuries - advice for development of joint protocols [The management of children with spinal cord injuries]. 2014. https://secure.rcem.ac.uk/ [internet publication].http://www.rcem.ac.uk/RCEM/Quality_Policy/Clinical_Standards_Guidance/Local_Guidance/RCEM/Quality-Policy/Clinical_Standards_Guidance/Local_Guidance.aspx?hkey=3765ca3b-617c-427c-a4af-57fca689a0de
膀胱扩张
脊髓休克期间膀胱会变得松弛,导致过度扩张,这可能会造成永久性的损害。 所有患者都需要导尿管,最初应设置为自由排尿。[73]London Spinal Cord Injury Centre, National Spinal Cord Injury Board. Spinal cord injuries - advice for development of joint protocols [The management of children with spinal cord injuries]. 2014. https://secure.rcem.ac.uk/ [internet publication].http://www.rcem.ac.uk/RCEM/Quality_Policy/Clinical_Standards_Guidance/Local_Guidance/RCEM/Quality-Policy/Clinical_Standards_Guidance/Local_Guidance.aspx?hkey=3765ca3b-617c-427c-a4af-57fca689a0de
自主神经反射障碍
自主神经反射异常是一种潜在的危险情况,可能发生于T6或更高脊髓节段损伤的患者,导致不受控制的高血压,进而导致癫痫、视网膜出血、脑出血,肺水肿、心肌梗死或肾功能损害。 病理生理机制涉及病变平面以下的刺激激活交感神经系统。 由于脊髓的不连续从而造成下行的抑制信号无法通过损伤的平面,因此中枢神经系统无法对激活的交感神经系统进行神经调节。 T6以下的病变通常可以通过足够的下行副交感神经抑制信号调节激活的交感神经张力。[74]Milligan J, Lee J, McMillan C, et al. Autonomic dysreflexia: recognizing a common serious condition in patients with spinal cord injury. Cam Fam Physician. 2012 Aug;58(8):831-5.http://www.cfp.ca/content/58/8/831.longhttp://www.ncbi.nlm.nih.gov/pubmed/22893332?tool=bestpractice.com
治疗包括处理造成刺激的根本原因,以及使用当地推荐的抗高血压药物。
其他治疗方式
过去曾推荐使用静脉滴注甲基泼尼松龙来治疗急性脊髓损伤。[75]Bracken MB, Collins WF, Freeman DF, et al. Efficacy of methylprednisolone in acute spinal cord injury. JAMA. 1984;251:45-52.http://www.ncbi.nlm.nih.gov/pubmed/6361287?tool=bestpractice.com[76]Bracken MB, Sheppard MJ, Collins WF, et al. A randomized, controlled trial of methylprednisolone or naloxone in the treatment of acute spinal-cord injury: results of the Second National Acute Spinal Cord Injury Study. New Engl J Med. 1990;322:1405-1411.http://www.ncbi.nlm.nih.gov/pubmed/2278545?tool=bestpractice.com[77]Bracken MB, Shepard MJ, Holford TR, et al. Administration of methylprednisolone for 24 or 48 hours or tirilazad mesylate for 48 hours in the treatment of acute spinal cord injury: results of the Third National Acute Spinal Cord Injury Randomized Controlled Trial. National Acute Spinal Cord Injury Study. JAMA. 1997;277:1597-1604.http://www.ncbi.nlm.nih.gov/pubmed/9168289?tool=bestpractice.com 但是,由于存在严重的不良反应(例如减缓创伤愈合、引起感染、死亡率增加),并且关于其使用的研究方法也有问题,所以这种药物的使用存在争议,并不认为这是一种受到推荐的标准治疗。[78]Hurlbert RJ, Moulton R. Why do you prescribe methylprednisolone for acute spinal cord injury? A Canadian perspective and a position statement. Can J Neurol Sci. 2002; 29:236-239.http://www.ncbi.nlm.nih.gov/pubmed/12195612?tool=bestpractice.com
 [Figure caption and citation for the preceding image starts]: 胸腰段椎体骨折的治疗B. Nurboja博士创建 [Citation ends].
[Figure caption and citation for the preceding image starts]: 胸腰段椎体骨折的治疗B. Nurboja博士创建 [Citation ends].