检查
首要检查
胸部 X 线检查(CXR)
如果病史和体格检查提示可能的原发部位,则诊断试验应重点关注该原发部位。但在绝大多数病例中,检查往往不那么具有导向性。传统上,胸部 X 线 (CXR) 检查被推荐为疑似 AUP 患者的初始放射影像学筛查。 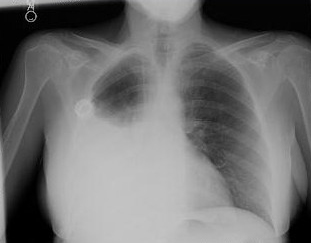 [Figure caption and citation for the preceding image starts]: AP CXR 揭示存在大量右侧胸腔积液和右颈内静脉 Medi-Port;胸膜液细胞检测提示腺癌,但常规病情检查期间未识别出任何原发部位;进一步成像揭示确实存在纵隔淋巴结肿大,开始化疗由 Dr D. Cosgrove 提供的个人资料 [Citation ends].
[Figure caption and citation for the preceding image starts]: AP CXR 揭示存在大量右侧胸腔积液和右颈内静脉 Medi-Port;胸膜液细胞检测提示腺癌,但常规病情检查期间未识别出任何原发部位;进一步成像揭示确实存在纵隔淋巴结肿大,开始化疗由 Dr D. Cosgrove 提供的个人资料 [Citation ends].
存在占位病变
CT(胸部、腹部、骨盆)
近期研究表明,使用胸部 CT 可提高诊断率,尤其是在诊断有单发 CNS 转移患者的小型、隐蔽性原发性病变时。[15] 腹部和骨盆 CT 扫描通常用于评估腹内疾病以及女性骨盆病变。  [Figure caption and citation for the preceding image starts]: 静脉使用对比剂的腹部 CT 显示,右侧肝叶有许多增强性病变,伴有腹水;对其中一个病变进行的经皮活检提示腺癌,但常规病情检查期间未识别出任何原发部位:典型的 AUP 表现由 Dr D. Cosgrove 提供的个人资料 [Citation ends].
[Figure caption and citation for the preceding image starts]: 静脉使用对比剂的腹部 CT 显示,右侧肝叶有许多增强性病变,伴有腹水;对其中一个病变进行的经皮活检提示腺癌,但常规病情检查期间未识别出任何原发部位:典型的 AUP 表现由 Dr D. Cosgrove 提供的个人资料 [Citation ends]. [Figure caption and citation for the preceding image starts]: 使用静脉对比剂的腹部 CT 显示,两侧肝叶有许多增强性肝病变;右侧肝叶的经皮活检显示腺癌由 Dr D. Cosgrove 提供的个人资料 [Citation ends].
[Figure caption and citation for the preceding image starts]: 使用静脉对比剂的腹部 CT 显示,两侧肝叶有许多增强性肝病变;右侧肝叶的经皮活检显示腺癌由 Dr D. Cosgrove 提供的个人资料 [Citation ends].
异常肿块
乳房 X 线检查
应对所有记录有腺癌的女性患者进行乳房 X 线检查,并且有孤立腋窝淋巴结肿大女性患者的乳腺癌疑似指数应该更高。如果乳房 X 线检查结果正常,则应在这些病例中考虑进行乳房 MRI。在筛查人群中,乳房 X 线检查的敏感性为 75%-90%,特异性为 90%~95%。[26] 尚未在 AUP 人群中对这些数据进行验证。
乳房 X 线检查显示存在肿块病变或微小钙化灶提示乳腺癌
乳房 MRI
应对所有乳房 X 线摄影检查结果正常或或无结论的腋淋巴结腺癌女性患者进行乳房 MRI。近期研究表明,MRI 在检测乳腺癌方面的敏感性略高于乳房 X 线摄影检查,但特异性略低。[27]
MRI 显示存在包块提示乳腺癌。
经阴道超声
对于有腹水的女性患者,这是首选的成像检查,可用于评估是否存在卵巢肿块。使用联合的手段进行检查(三维形态学联合彩色血流多普勒成像)时,在筛查人群中识别卵巢病变的敏感性超过 90%。尚未在 AUP 人群中验证这些数据。[28]
存在附件肿块提示卵巢癌
诊断性穿刺
应对所有有腹水但无其他部位疾病证据的患者进行诊断性穿刺,以记录腺癌的存在。较大体积(大于 1 L)的穿刺可提高诊断率。对于女性患者,有乳头状特征的腹膜腺癌是有利的临床病理亚型,可通过穿刺对其进行识别。[29]
腹膜液中存在腺癌细胞
上呼吸消化道广视野内镜检查(用于有孤立颈淋巴腺病的患者)
可对所有记录为腺癌的颈链淋巴结肿大患者进行该检查。应对识别的病变进行活检,以确认与转移病灶的病理一致。该检查操作的敏感性估计值差异较大,有些专家用更可靠的影像学检查方法的出现来质疑创伤性检查的必要性。[30]
头/颈部 CT 扫描结合 PET 可提供额外的信息,以获得更好的颈淋巴结成像。
原发性头颈癌、食道癌或肺癌的黏膜病变可视化
需要考虑的检查
结肠镜检查(用于有可切除肝转移的患者)
应对所有记录为腺癌的可切除肝脏转移患者进行结肠镜检查。结肠镜检查可识别各种黏膜病变,为了确认与转移病灶的病理一致性,活检必不可少。结肠镜检查用于检测结直肠癌的敏感性为 95%,特异性近 100%,因为可视化病变的病理评估被认为是最精确的诊断性检查。
显示结直肠癌的黏膜病变
光学显微镜检查结合苏木素和伊红 (H&E) 染色
在从最容易进入的转移病灶中获取的所有肿瘤标本上进行。
腺结构的分化程度由病理科医生确定,通常分为分化良好、中度分化、分化不良或未分化。
腺形成且存在黏蛋白
免疫组织化学 (IHC) 标志物
用于对腺癌细胞进行进一步分类,以识别可能的肿瘤起源部位。鉴别流程基于细胞角蛋白染色、CK7 和 CK20。[1] 单个抗原表达为阳性或阴性。[13]
在该初始流程后可使用更具有特异性的 IHC 标志物,例如用于尿路上皮癌的 UROIII;用于肺腺癌或甲状腺瘤的 TTF-1;用于肝细胞癌的 Hep par-1;用于前列腺癌的 PSA;用于乳腺癌的 ER(雌激素受体)、PR(孕激素受体)、Her-2 neu 及 GCDFP-15;以及用于胆管癌的 CK19。[14] 应根据初始诊断性病情检查的指标及向病理学家的咨询安排特异性检查。
原发性病变和转移性病变中的 IHC 标志物偶尔会有区别,这意味着转移性病变的 IHC 标志物组合检查不总是与其原发部位相同。[16] 基因表达谱分析提示,原发部位不明的癌症可能会隐藏与原发灶已知肿瘤不同的分子/基因特性。[17] 这可能归因于分子学分类错误、尸检中的药物难以到达渗透部位 (sanctuary site),或者假设的促转移基因特征。[18]
通过标志物的抗体识别特异性肿瘤抗原
雌激素和孕激素受体状态
应对所有女性腺癌患者,尤其是有孤立腋窝淋巴结肿大的女性患者,进行 ER(雌激素受体)和 PR(孕激素受体)的免疫组织化学标志物。表达这些受体的肿瘤对激素疗法敏感。
非乳腺/妇科起源的癌症中,偶尔可看到 ER 和 PR 表达,为此,原发部位不明癌中的转移性乳房、卵巢或子宫内膜癌的诊断不应完全基于 ER 和 PR 的表达。[31]
通过标记的抗体识别特异性肿瘤受体
血清肿瘤标志物
这些应在某些临床环境中进行评估,阳性结果被记录为在所定义的参考范围之外。
对于有记录的腺癌和骨骼转移的男性患者,检测血清 PSA。升高的 PSA 被定义为大于 4 μg/L(大于 4 ng/mL),PSA 值越高,则与前列腺癌的相关性更明确。作为筛查试验,PSA 检测结果处于这一水平时,诊断前列腺癌的敏感性为 80%~95%,特异性为 10%~20%。有人正在对 PSA 亚型检测进行研究,以作为一种提高该试验特异性的方法。[32]
对于有分化不良癌的男性患者,尤其是有中线肿瘤的年轻男性患者,检测血清 AFP 和 β-hCG。在该患者人群中,AFP 大于 6 μg/L(大于6 ng/mL)、β-hCG 大于 10 IU/L 提示生殖细胞肿瘤。
可显示升高的 PSA、AFP 或 β-hCG
新兴检查
正电子发射断层成像 (positron emission tomography, PET)
近年来,PET 已被广泛评估为 AUP 诊断工具,无论是单独使用还是与 CT 联合(以产生组合的功能解剖影像)使用。这些数据表明,进行 PET 或 PET/CT 扫描的患者的原发肿瘤部位以及其他转移灶的识别率增高,[21] 但是,与其他方法相比,假阳性率似乎增加。[22] 有证据表明,治疗决策受 PET 或 PET/CT 结果影响,但缺乏有关基于该影响的总生存数或这些工具在治疗 AUP 时成本效益的数据。
当患者具有单一位点疾病且已有以治愈为目的计划时,PET 尤其有用。[23]
可识别原发肿瘤部位或其他转移灶
基因表达谱
使用此内容应接受我们的免责声明。
