病史和查体
关键诊断因素
存在的危险因素
高危因素包括:肥胖;青春期状态;印度-亚裔或黑色人种;阳性家族史/遗传倾向。
黑棘皮症
存在于90%-95%的患者中。[57]
胰岛素抵抗的皮肤表现就是皮肤色素沉着,常发生在易摩擦部位。  [Figure caption and citation for the preceding image starts]: 黑棘皮症来自Jennifer Miller博士 [Citation ends].
[Figure caption and citation for the preceding image starts]: 黑棘皮症来自Jennifer Miller博士 [Citation ends].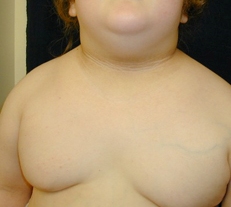 [Figure caption and citation for the preceding image starts]: 一个肥胖儿童患黑棘皮病来自Jennifer Miller博士 [Citation ends].
[Figure caption and citation for the preceding image starts]: 一个肥胖儿童患黑棘皮病来自Jennifer Miller博士 [Citation ends].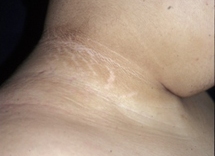 [Figure caption and citation for the preceding image starts]: 黑棘皮病易出现在颈部褶皱处来自Jennifer Miller博士 [Citation ends].
[Figure caption and citation for the preceding image starts]: 黑棘皮病易出现在颈部褶皱处来自Jennifer Miller博士 [Citation ends].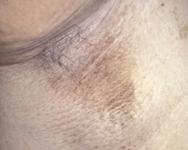 [Figure caption and citation for the preceding image starts]: 在腋下黑棘皮病来自Jennifer Miller博士 [Citation ends].
[Figure caption and citation for the preceding image starts]: 在腋下黑棘皮病来自Jennifer Miller博士 [Citation ends].
不是2型糖尿病的特异性表现,也可在一些1型糖尿病合并肥胖的患儿中发现。
多尿
通常出现在空腹血糖>16.7 mmol/L (>300 mg/dL) 和/或糖化血红蛋白 (HbA1c) >86 mmol/mol (>10%) 的患者中。
多饮
通常出现在患者空腹血糖大于16.7 mmol/L (>300 mg/dL) 和/或HbA1c 大于86 mmol/mol (>10%)。
夜尿
由高血糖导致的利尿。
其他诊断因素
危险因素
肥胖
遗传素质
高风险的种族背景
大部分儿童发病的2型糖尿病患者有高危种族背景[11][12] 在美国,从1990-1998年间,美国印第安人和阿拉斯加本土儿童的2型糖尿病患病率增长了71%。[11] 尽管不同国家的种族背景各不相同,但是全球中印度-亚洲人的种族背景风险最高。[13] 与白种儿童比较,这些印度-亚洲人的祖先患肥胖、胰岛素抵抗、代谢紊乱的年龄较早,与同BMI的人相比,中心性肥胖的趋势更明显。[14] 在南加利福尼亚州,三分之一的墨西哥裔美国人儿童和青年患糖尿病,在德克萨斯州南部三分之二的这些患儿为2型糖尿病。[15][16] 在辛辛那提,阿肯色州和德克萨斯州,黑人儿童2型糖尿病的患者占70%-75%,表明不同种族背景的胰岛素敏感性存在差异。[17][18] 调整体重、年龄、青春期这些因素后,与白人儿童相比较,黑人儿童在青春前期及青春期口服葡萄糖对空腹及胰岛素的刺激更大,脂肪分解更少。[49]
青春期
青春期与胰岛素抵抗相关,反映在口服或静脉注射葡萄糖后患者胰岛素的峰值增加2-3倍,胰岛素介导的血糖代谢下降30%。[33] 青春期可能加剧预先存在胰岛素抵抗患者的β细胞功能的衰竭情况。
早产儿
子宫内环境引发胎儿生长受限及营养受限,导致儿童β细胞功能下降,诱发外周组织胰岛素抵抗。[38]
婴儿期快速增长
糖尿病患者子宫内环境
儿童曾暴露在糖尿病母亲子宫内,后天获得糖尿病的危险度较未暴露在糖尿病子宫内环境的兄弟姐妹高3.7倍。[37]
人工喂养
与人工喂养相比,母乳喂养减少肥胖儿童相对危险度达20%。[42] 人工喂养与过度喂养有关。 母乳喂养在儿童发育的关键阶段提供更加合理的热量摄入。
婴儿的高蛋白摄取
多囊卵巢
与胰岛素抵抗及高胰岛素血症相关,这些都易诱发2型糖尿病。
肌细胞内脂质含量
在体内及体外研究的数据表明骨骼肌神经酰胺增加可损伤胰岛素的作用,从而降低骨骼肌对血糖的摄取。[47]
脂肪沉积于肝脏
谷丙转氨酶增加与肝脏胰岛素敏感性下降与2型糖尿病的发病相关。[48]
使用此内容应接受我们的免责声明。
